BCCSA抑菌剂(1ml*5)/每200ml洋葱伯克霍尔德菌群选择性琼脂培养基(BCCSA)中加入1支BCCSA抑菌剂


![]()
-
平板计数琼脂(PCA)(颗粒剂型)
GCM101 | 详见说明
-
ACHN细胞培养基
BNCC368102 | 见详情
-
TCBS琼脂
BNCC378061 | 见详情
-
ACHN细胞培养基
BNCC380025 | 见详情
-
CASO液体培养基
BNCC381105 | 见详情
-
CASO琼脂
BNCC384438 | 见详情
-
DH10Bac大肠杆菌
BNCC353824 | 见详情
-
Middle Brook 7H9+25μg/mL卡那霉素液体培养基
BNCC393079 | 见详情
-
改良PYG+瘤胃液(30ml/L)
BNCC391263 | 见详情
-
DSMZ培养基339液体试管
BNCC392972 | 见详情
-
MOC1细胞专用培养基
BNCC389085 | 见详情
-
R2A液体培养基
BNCC392990 | 见详情




用法:
每200ml洋葱伯克霍尔德菌群选择性琼脂培养基(BCCSA)中加入1支BCCSA抑菌剂(含庆大霉素2mg,万古霉素0.5mg,多粘菌素B120000U)
BCCSA抑菌剂(1ml*5)微生物灵敏度试验:
按标签用法制备培养基,接种以下质控菌株。放置30-35℃需氧培养48-72小时。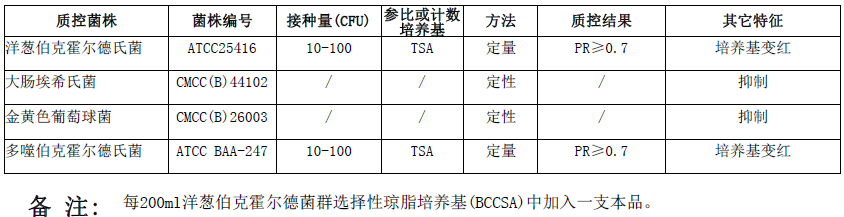
以上信息仅供参考,请以实物批次为准!
本公司销售的所有产品仅供实验科研使用,不用于人体及临床诊断。
适用于消毒剂与抗抑菌剂中抗菌药物(如磺胺类、喹诺酮类等)的定性及定量检测,涵盖液体、凝胶、粉剂等剂型[4]。
采用液相色谱-质谱联用技术(LC-MS/MS),通过离子对模式分离目标物,结合内标法定量[4][5]。
磺胺类化合物检出限为0.05 μg/mL,定量限为0.1 μg/mL;喹诺酮类检出限为0.02 μg/mL,定量限为0.05 μg/mL[4]。
需包含空白样品、加标回收样品(低、中、高浓度)及阳性对照样品,加标回收率应控制在80%~120%[4][5]。
1. 样品前处理:超声提取后离心过滤;
2. 色谱条件:C18色谱柱,流动相为甲醇-0.1%甲酸水溶液;
3. 质谱参数:电喷雾电离(ESI+),多反应监测模式(MRM)[4][5]。
检测中需使用特异性中和剂消除样品基质干扰,如硫代硫酸钠或卵磷脂吐温80溶液[4][5]。
规范含抑菌成分的一次性卫生用品(如湿巾、卫生棉)的微生物限值及抑菌性能评价[5]。
采用平皿计数法测定细菌菌落总数,抑菌率通过振荡烧瓶法或奎因试验法评价[5]。
细菌总数检出限为10 CFU/g,定量限为20 CFU/g;抑菌率≥90%为合格[5]。
需包含阴性对照(无菌生理盐水)和阳性对照(标准菌株接种样品),平行实验3次[5]。
1. 样品预处理:无菌条件下剪碎并稀释;
2. 培养条件:37℃恒温培养48小时;
3. 结果计算:抑菌率=(对照组菌落数-实验组菌落数)/对照组菌落数×100%[5]。
若样品含乙醇等挥发性成分,需在检测前静置24小时以消除干扰[5]。
适用于添加抑菌成分的液体、粉状洗涤剂产品,包括衣物、餐具类抑菌剂[4]。
抑菌性能采用最小抑菌浓度(MIC)法,通过二倍稀释法测定对金黄色葡萄球菌、大肠杆菌的抑制效果[4]。
MIC值≤1.0%为有效抑菌浓度,定量限为0.5%[4]。
需使用标准菌株(ATCC 25922大肠杆菌、ATCC 6538金黄色葡萄球菌)及空白对照[4]。
1. 菌悬液制备:0.5麦氏比浊度;
2. 稀释梯度:1%~0.0625%浓度梯度;
3. 结果判定:无可见菌生长的最低浓度为MIC值[4]。
若产品含氧化性成分(如次氯酸钠),需预先中和处理以避免假阴性结果[4]。
以上信息仅供参考,请以相应标准的原文为准!